동맥관 개존
Patent ductus arteriosus
동맥관 개존의 개요
사진 설명을 입력하세요.
▴ 그림 30. 동맥관 개존(c)
a-우심방, b-대동맥, c-동맥관 개존, d-폐동맥, e-폐정맥, f-좌심방, g-좌심실, i-우심실
Copyright ⓒ 2011 John Sangwon Lee, MD, FAAP
● 출생 전 태아의 대동맥과 폐동맥 사이에 연결된 짤막한 혈관이 하나가 정상적으로 있다.
● 이 혈관을 동맥관이라고 한다(그림 10 태아의 혈액 순환도, 그림 30, 31, 32 참조).
● 출생 전 태아들의 정상 혈액순환은 출생 후 신생아들을 비롯한 영유아들, 학령기 아이들, 사춘기 아이들, 성인들의 정상 혈액순환과 다른 점이 많다.
● 출생 전 태아들의 폐동맥과 대동맥을 연결하는 동맥관이 개존되어 있고 또 우심방과 좌심방 사이 심방 중격에 난원공이 정상적으로 있다.
● 태어난 후, 정상적으로 우심실 속 정맥혈의 전부가 폐동맥을 거쳐 폐 속으로 흘러간다.
● 그러나 태어나기 전 태아의 경우, 우심실 속에 있는 모든 혈액이 일단 폐동맥 속으로 흘러 가다가 그 혈액의 일부는 나머지 폐동맥 속을 계속 통과한 다음 마지막으로 폐 속으로 흘러가고
● 나머지 부분의 혈액은 동맥관을 통과해서 대동맥 속으로 흘러 들어가는 것이 정상 태아혈액 순환과정이다.
● 그렇지만 출생 후 바로 동맥관은 정상적으로 저절로 막히고 우심실 속 정맥혈의 전부가 폐동맥을 거쳐 속으로 흘러간다. 이 때는 우심실에서 흘러온 폐동맥 속 혈액이 정상적으로 막힌 동맥관을 통과해서 대동맥 속으로 더 이상 흘러갈 수가 없다(그림 10 태아 혈액 순환도 참조).
● 그러나 드물게, 출생 후 동맥관이 완전히 막히지 않고 계속 열려 있는 경우가 있다.
● 이런 혈관 기형을 동맥관 개존이라고 하고 그로 인해 생긴 증상 징후를 동맥관 개존증이라 한다.
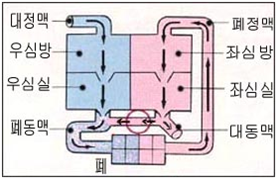
사진 설명을 입력하세요.
그림 32. 동맥관 개존
◯로 표시된 부위에 있는 동맥관 개존
Copyright ⓒ 2011 John Sangwon Lee, MD, FAAP
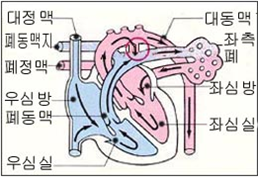
사진 설명을 입력하세요.
그림 31. 동맥관 개존
◯로 표시된 부위에 있는 동맥관 개존
Copyright ⓒ 2011 John Sangwon Lee, MD, FAAP
■ 동맥관 개존의 원인
● 원인은 아직 확실히 모른다.
● 임신 첫 3개월에 임신부가 풍진을 앓을 때 태아도 풍진바이러스에 감염되면 풍진에 걸릴 수 있고 동맥관이 출생 후 계속 개존될 수 있다.
● 또 특히 체중이 1,500∼1,750g 정도 되는 아주 작은 미숙 신생아들의 15%에서 출생 후 얼마 동안 동맥관이 일시적으로 개존되어 있을 수 있다.
● 출생 후 동맥관이 계속 개존되어 있을 때는 대동맥 속 동맥혈이 동맥관을 통과해서 폐동맥 속으로 흘러들어간다.
● 태어나기 전과 정반대의 동맥관 혈액 순환 과정이 생기는 셈이다.
● 대동맥 속 혈액이 동맥관 속을 통과해서 흘러간 폐동맥 속 동맥혈과 우심실 속에서 폐동맥 속으로 흘러 들어온 정맥혈이 섞인 동맥혈, 정맥혈이 폐동맥 속을 통과 해 폐 속으로 흘러 들어간다.
● 따라서 동맥관 개존이 있을 때 폐가 정상 이상으로 더 많은 혈액 양을 취급해야 하는 부담을 갖게 된다.
● 이런 이유로, 심장은 정상 이상으로 더 많은 혈액 양을 펌프하게 되고 심장 전체가 보통 이상으로 더 많은 펌프 부담을 갖게 된다.
● 결국 좌심방과 좌심실이 비정상적으로 더 커질 수 있고 좌 폐동맥 분지맥과 우 폐동맥 분지맥의 혈압이 비정상적으로 더 상승되고 그에 따른 여러 가지 증상 징후가 생길 수 있다.
■ 동맥관 개존의 증상 징후
● 대부분의 큰 미숙 신생아들이나 정상 분만으로 태어난 만삭 신생아들에게 동맥관 개존이 있어도 그로 인해 생후 얼마 동안은 아무 증상 징후가 나타나지 않을 수 있다.
● 아주 작은 미숙 신생아에게 동맥관 개존이 있을 때는 그런 미숙 신생아에게 특발성 호흡곤란 증후군, 폐렴 또는 그 외 다른 종류의 폐 질환이 더 쉽게 생길 수 있고 그로 인해 심부전증이 더 쉽게 생길 수 있고, 호흡곤란도 더 심하게 생길 수 있다.
● 동맥관 개존이 없는 신생아들의 경우, 좌심실 속 전체 혈액이 대동맥을 통과해서 전신으로 흘러가는 것이 정상이다.
● 그렇지만, 출생 후, 동맥관 개존이 그대로 계속 있을 때는 좌심실 속 동맥혈의 전부가 동맥관 개존이 있는 바로 전 대동맥 부위까지 정상적으로 흘러가지만 동맥관 개존이 있는 대동맥 부분에 도달하면 대동맥 속 동맥혈의 전체 혈 양 중 일부는 개존 동맥관 속을 통과한 다음 주 폐동맥 속으로 들어간 후 좌우 폐동맥 분지를 거쳐 폐포 모세혈관까지 계속 흘러 들어간다.
● 그리고 좌심실 속에서부터 동맥관의 한끝이 붙은 대동맥 속 부분까지 흘러온 대동맥 속 혈액의 전 양 중 나머지의 혈액(동맥관 속을 통과해서 폐 속으로 들어가지 않은 나머지 대동맥 혈)은 나머지 대동맥으로 계속 흘러간다.
● 이때 전체 심장이 정상 이상으로 혈액을 더 많이 펌프해야 한다. 그 때문에 심장이 피를 펌프하는 데 보통 이상으로 더 부담을 갖게 된다.
● 그래서 심장이 더 커지고 때로는 심부전증이 생길 수 있다.
● 적절히 치료하지 않으면 숨이 가쁘고 성장 발육이 부진할 수 있다.
● 드물게 왼쪽 앞가슴이 아프고 목이 쉴 수 있다.
■ 동맥관 개존의 진단
● 병력, 증상 징후, 진찰소견 등을 종합하여 이 병이 있다고 의심하면 심전도 검사, 가슴 X-선 사진 검사, 심초음파 검사, 심음도 검사, 심도자법 검사 등으로 쉽게 진단할 수 있다.
■ 동맥관 개존의 치료
● 동맥관 개존이 있지만 증상 징후가 거의 없거나 조금 있을 때는 2~4세가 될 때까지 기다렸다가 선택적 동맥관 개존 수술 치료를 한다. 이 수술 방법은 비교적 간단하고 쉽다. 단 한 번 수술로 완치시킬 수 있다.
● 심부전증이 동맥관 개존으로 생기거나 생명에 위험한 증상이 나타나면, 심부전증을 약물로 적절히 치료하다가 대개 2세가 되기 전 적절한 시기에 선택적 수술 치료를 한다.
● 동맥관 개존이 있는 아주 작은 미숙 신생아가 특발성 호흡곤란 증후군이나 그 외 다른 종류의 폐 질환을 앓을 때는 동맥관 개존의 증상 징후가 더 심할 수 있다. 그때 폐질환의 중증도가 더 심할 수 있다.
● 이 때문에 동맥관 개존을 응급으로 수술 치료할 때도 있다.
● 수술 치료를 하는 대신 인도메사신(Indomethacin) 제도로 개존된 동맥관은 내과적 치료를 하기도 한다.
● 요즘은 동맥관 개존을 혈관 카테터로 치료하기도 한다.
● 동맥관 개존이 있으면 폐렴에 더 잘 걸릴 수 있고, 감염병을 경미하게 앓아도 심부전증이 생기기 쉽기 때문에 감염병을 앓을 때는 곧 치료를 받아야 한다.
● 인도메사신(Indomethacin) 치료하는 대신 경구용 Ibuprofen(15~25 mg/kg)으로 최초 치료하고 난 후 매 12시간 내지 24시간마다 7.5 mg-15 mg/kg을 3번 치료한 결과가 좋다고 한다. 소스: NEJM Journal Watch, June 2018.
Copyright drleepediatrics.com 2/28/2020
Patent Ductus Arteriosus
Overview of Patent Ductus Arteriosus
[Insert Image Caption]▴ Figure 30. Patent Ductus Arteriosus (c)
a—Right Atrium, b—Aorta, c—Patent Ductus Arteriosus, d—Pulmonary Artery, e—Pulmonary Vein, f—Left Atrium, g—Left Ventricle, i—Right Ventricle
Copyright ⓒ 2011 John Sangwon Lee, MD, FAAP
● Prior to birth, a fetus normally possesses a short blood vessel connecting the aorta and the pulmonary artery.
● This vessel is called the ductus arteriosus (see Figure 10: Fetal Blood Circulation Diagram, and Figures 30, 31, and 32).
● The normal pattern of blood circulation in a fetus prior to birth differs significantly from the normal circulation found after birth in newborns, infants and toddlers, school-aged children, adolescents, and adults.
● In the fetus prior to birth, the ductus arteriosus—which connects the pulmonary artery and the aorta—remains open (patent); additionally, a small opening known as the foramen ovale is normally present within the atrial septum (the wall separating the right and left atria).
● After birth, under normal circumstances, the entirety of the venous blood from the right ventricle flows through the pulmonary artery and into the lungs.
● However, in the case of a fetus prior to birth, all the blood within the right ventricle initially flows into the pulmonary artery; a portion of this blood continues through the pulmonary artery to eventually reach the lungs,
● while the remaining portion of the blood passes through the ductus arteriosus and flows into the aorta—this constitutes the normal process of fetal blood circulation.
● Nevertheless, immediately after birth, the ductus arteriosus normally closes spontaneously, and the entirety of the venous blood from the right ventricle subsequently flows through the pulmonary artery and into the lungs. At this stage, the blood flowing from the right ventricle into the pulmonary artery can no longer pass through the now-closed ductus arteriosus to enter the aorta (refer to Figure 10: Fetal Blood Circulation Diagram).
● However, in rare cases, the ductus arteriosus fails to close completely after birth and remains open.
● This vascular malformation is referred to as a *patent ductus arteriosus* (PDA), and the signs and symptoms resulting from it constitute the clinical condition known as *patent ductus arteriosus*.
[Enter photo caption here]
Figure 32. Patent Ductus Arteriosus
The patent ductus arteriosus is located in the area marked by a circle (◯).
Copyright ⓒ 2011 John Sangwon Lee, MD, FAAP
[Delete main image] [Enter photo caption here]Figure 31. Patent Ductus Arteriosus
The patent ductus arteriosus is located in the area marked by a circle (◯).
Copyright ⓒ 2011 John Sangwon Lee, MD, FAAP
■ Causes of Patent Ductus Arteriosus
● The exact cause remains unknown.
● If a pregnant woman contracts rubella (German measles) during the first trimester of pregnancy, the fetus may also become infected with the rubella virus; this can lead to congenital rubella in the fetus and may result in the ductus arteriosus remaining open after birth.
● Additionally—particularly in very small premature infants weighing approximately 1,500 to 1,750 grams—the ductus arteriosus may remain temporarily open for a period of time after birth in about 15% of cases.
● When the ductus arteriosus remains open after birth, oxygenated blood from the aorta flows through the ductus arteriosus into the pulmonary artery.
● This effectively creates a pattern of blood circulation through the ductus arteriosus that is the exact opposite of the circulation pattern observed before birth. ● Blood flowing through the aorta passes through the ductus arteriosus and enters the pulmonary artery; here, this arterial blood mixes with the venous blood that has flowed from the right ventricle into the pulmonary artery. Consequently, this mixture of arterial and venous blood flows through the pulmonary artery and into the lungs.
● Therefore, when a patent ductus arteriosus (PDA) is present, the lungs are burdened with the task of handling a volume of blood that exceeds normal levels.
● For this reason, the heart is compelled to pump a greater volume of blood than is typical, placing an excessive pumping burden on the entire heart.
● Ultimately, the left atrium and left ventricle may become abnormally enlarged; furthermore, blood pressure within the left and right pulmonary artery branches may rise to abnormal levels, potentially leading to the manifestation of various associated signs and symptoms.
■ Signs and Symptoms of Patent Ductus Arteriosus (PDA)
● In most large premature infants—as well as in full-term infants born via normal delivery—the presence of a patent ductus arteriosus may not result in any observable signs or symptoms for a period following birth.
● In very small premature infants, however, the presence of a patent ductus arteriosus increases susceptibility to conditions such as idiopathic respiratory distress syndrome, pneumonia, or other pulmonary diseases. This, in turn, heightens the risk of developing heart failure and can lead to more severe respiratory distress.
● In newborns without a patent ductus arteriosus, the normal physiological state is for the entire volume of blood within the left ventricle to flow through the aorta and circulate throughout the systemic circulation. ● However, if the ductus arteriosus remains open after birth, the entire volume of oxygenated blood from the left ventricle flows normally up to the section of the aorta immediately preceding the open duct. Upon reaching the aortic segment containing the open duct, a portion of the total aortic blood volume passes through the ductus arteriosus, enters the main pulmonary artery, and continues flowing through the left and right pulmonary artery branches into the alveolar capillaries.
● Meanwhile, the remaining portion of the aortic blood—that is, the blood that did not pass through the ductus arteriosus into the lungs—continues to flow onward through the rest of the aorta.
● Consequently, the entire heart is forced to pump a volume of blood exceeding its normal capacity. This places an increased workload and strain on the heart as it performs its pumping function.
● As a result, the heart may enlarge, and in some cases, congestive heart failure may develop.
● If left untreated, symptoms such as shortness of breath and delayed growth and development may occur.
● Rarely, patients may experience pain in the left side of the chest or hoarseness.
■ Diagnosis of Patent Ductus Arteriosus
● If, based on a comprehensive assessment of the patient’s medical history, signs and symptoms, and physical examination findings, there is a suspicion that this condition is present, a definitive diagnosis can be easily established through tests such as an electrocardiogram (ECG), chest X-ray, echocardiogram, phonocardiogram, or cardiac catheterization.
■ Treatment of Patent Ductus Arteriosus
● In cases where patent ductus arteriosus is present but symptoms are minimal or entirely absent, surgical intervention is typically deferred until the child reaches 2 to 4 years of age, at which point elective surgical closure of the ductus arteriosus is performed. This surgical procedure is relatively simple and straightforward; a complete cure can be achieved with a single operation. ● If heart failure develops as a result of patent ductus arteriosus (PDA), or if life-threatening symptoms emerge, the heart failure is appropriately managed with medication; subsequently, elective surgical treatment is typically performed at an appropriate time, usually before the child reaches the age of two.
● In very small premature infants with PDA, symptoms and signs of the condition may be more severe if the infant is also suffering from idiopathic respiratory distress syndrome or other types of pulmonary disease. In such cases, the severity of the underlying lung disease itself may also be exacerbated.
● For this reason, emergency surgical intervention for PDA is sometimes required.
● As an alternative to surgical treatment, medical management using Indomethacin may be employed to close the patent ductus arteriosus.
● Nowadays, PDA is also frequently treated using vascular catheterization techniques.
● Because the presence of PDA increases susceptibility to pneumonia and makes the development of heart failure more likely—even in the case of a mild infection—it is imperative to seek immediate medical attention whenever an infection occurs.
● It has been reported that an effective alternative to Indomethacin therapy involves initiating treatment with an oral dose of Ibuprofen (15–25 mg/kg), followed by three subsequent doses of 7.5–15 mg/kg administered every 12 to 24 hours. Source: NEJM Journal Watch, June 2018.
Copyright drleepediatrics.com 2/28/2020